일반 이름
데소게스트렐
에티닐에스트라디올 경구 피임제는 HIV 감염(에이즈) 및 다른 성 감염증(예를 들어 매독, 생식기 헤르페스, 임병, 클라미디아 감염증, 첨강 컨딜로마, 질 트리코모나스증, B형 간염 등)을 예방하는 것으로는 이런 감염을 예방하기 위해서는 콘돔 사용이 효과적임을 복용자에게 충분히 설명할 것.
또한 필요에 따라 성 감염증 검사의 실시를 고려할 것.
禁忌(다음 환자에게는 투여하지 않을 것)
1. 이 약의 성분에 과민성 소인이 있는
여성 일이 있다. ]
3. 진단이 확정되지 않은 이상성기 출혈이 있는 환자 [성기암의 의심이 있다. 출혈이 생식기 암으로 인한 경우 암의 악화 또는 현성화를 촉진 할 수 있습니다. 4. 혈전 성
정맥염, 폐색전증, 뇌혈관장애, 관상동맥질환 또는 그 기왕력이 있는 환자[혈액응고능이 항진되어 이들 증상이 악화될 수 있다. 5. 35세 이상으로 하루 15개 이상의 흡연자[심근경색 등 의
심혈관계 장애가 발생하기 쉬워진다는 보고가 있다. 6. 전조 (
섬광암점, 별형섬광 등)를 동반한 편두통 환자 있다. 7. 폐고혈압증 또는 심방세동 을
합병하는 심장막막증 환자, 아급성 세균성 심내막염의 기왕력이 있는 심장막막증 환자 [혈전증 등 심혈관계 장애가 발생 쉬워진다는 보고가 있다. 8. 혈관 병변 을
수반하는 당뇨병 환자(당뇨병성 신증, 당뇨병 망막증 등)[혈전증 등의 심혈관계의 장애가 발생하기 쉬워진다는 보고가 있다. 9. 혈전 성
소인이 있는 여성[혈전증 등의 심혈관계의 장애가 발생하기 쉬워진다는 보고가 있다. 10. 항인지질 항체 증후군 의
환자 [혈전증 등의 심혈관계의 장애가 발생하기 쉬워진다는 보고가 있다. 11. 수술 전 4주 이내 ,
수술 후 2주 이내, 산후 4주 이내 및 장기간 안정 상태의 환자[혈액 응고능이 항진되어 심혈관계의 부작용의 위험성이 높아질 수 있다. ]
12. 심각한 간장애가 있는 환자
13. 간종양 환자 [증상이 악화될 수 있음. 14. 지질대사 이상이 있는 환자[혈전증 등 의
심혈관계의 장애가 발생하기 쉬워진다는 보고가 있다. 또한 지질 대사에 영향을 미칠 수 있으므로 증상이 악화 될 수 있습니다. 15. 고혈압이 있는 환자 (
경증 고혈압 환자 제외) [혈전증 등 심혈관계 장애가 발생하기 쉬워진다는 보고가 있다. 또한 증상이 악화 될 수 있습니다.
16. 귀경화증 환자 [증상이 악화될 수 있음 ]
17. 임신 중에 황달, 지속성 소양증 또는 임신 헤르페스의 기왕력이 있는 환자 [증상이 재발할 우려가 있다 . ]
18. 임산부 또는 임신할 가능성이 있는 여성
19. 수유부
20. 뼈 성장이 종료되지 않았을 가능성이 있는 여성 [골단의 조기 폐쇄를 올 우려가 있다. ]
21. 옴비타스빌 수화물·파리타프레비르 수화물·리토나비르 배합제를 투여 중인 환자
효능 또는 효과
피임
효능 또는 효과와 관련된 주의
- 이 약은 다른 경구 피임제의 투여가 적절하지 않다고 생각되는 경우 투여를 고려한다. 레보놀게스트렐과 같은 경구 피임제와 비교하여 정맥 혈전증의 상대 위험률을 증가시키는 것을 시사하는 보고가 있다.
- 경구 피임제 사용 개시 1년간의 음주 잊음을 포함한 일반적인 사용에 있어서의 실패율은 9%라고 보고가 있다.
용법 및 용량
- <21정 제제>
1일 1정을 매일 일정 시간에 총 21일 연속 경구 투여한 후, 7일간 휴약한다. 유사한 방식으로 피임 기간 동안 반복적으로 투여한다.
- <28정 제제>
1일 1정을 매일 일정 시간에 백색정을 21일간 연속 경구 투여하고, 계속해서 녹색정을 7일간, 총 28일간 연속 투여한다. 다음 주기 이후에는, 소퇴 출혈의 유무에 관계없이, 계속 백색 정제로부터 투여를 개시하고, 28일간 연속 투여한다. 따라서, 1주기째의 투여 개시보다 휴약 기간은 일절 취하지 않는다. 통상, 녹색 정제 복용 중에 월경(소퇴 출혈)이 발래한다.
용법 및 용량과 관련된 주의
- 매일 일정한 시간에 복용시키는 것.
- 복용 개시일
경구 피임제를 처음 복용하는 경우, 월경 제1일째부터 복용을 개시하는 것. 복용 개시일이 월경 1일째부터 늦은 경우, 임신할 가능성이 있으므로, 마시기 처음의 1주일은 다른 피임법을 병용하는 것. - 본제의 투여에 있어서는, 음주 잊음 등이 없도록 복용 방법 등을 충분히 지도하는 것. 만일 마시는 것을 잊었을 경우(28정제제의 녹색정을 제외한다), 다음날까지 깨달았다면 즉시 마시는 것을 잊은 정제를 복용하고, 그 날의 정제도 통상대로 복용시킨다. 2일 이상 연속해서 마시는 것을 잊어버린 경우 복용을 중지시키고 다음 월경을 기다리고 투여를 재개시키는 것.
덧붙여 음주 잊음에 의해 임신할 가능성이 높아지므로, 그 주기는 다른 피임법을 사용시키는 것. - 다른 경구 피임제에서 본제로 전환하는 경우
- 21정 타입의 경구 피임제로부터 전환하는 경우
전에 복용하고 있던 약제를 모두 복용하고 7일간의 휴약 후, 계속해서 본제의 복용을 개시시킨다. 복용 개시가 지연되면 임신의 가능성이 있다. - 28정 타입의 경구 피임제로부터 전환하는 경우
전에 복용하고 있던 약제를 모두 복용 후, 계속해서 본제의 복용을 개시시킨다. 복용 개시가 지연되면 임신의 가능성이 있다.
- 21정 타입의 경구 피임제로부터 전환하는 경우
중요한 기본주의
- 본제의 복용에 의해, 연령, 흡연, 비만, 가족력 등의 리스크 인자의 유무에 관계없이 혈전증이 나타날 수 있으므로, 다음과 같은 증상이 나타난 경우는 즉시 투여를 중지해, 적절한 조치를 취할 것.
- 긴급 대응이 필요한 혈전증의 주요 증상
- 하지의 급격한 통증 · 부종, 갑작스런 호흡 곤란, 흉통, 심한 두통, 사지의 탈력 · 마비, 구문 장애, 급성 시력 장애 등
- 긴급 대응이 필요한 혈전증의 주요 증상
- 본제 복용자에 대해서도, 이러한 증상이 나타난 경우는, 즉시 복용을 중지해, 구급 의료 기관을 진찰하도록 설명하는 것.
- 이 약을 복용하는 동안 혈전증이 의심되는 증상이 나타나면 투여를 중단하는 등 적절한 조치를 취할 것.
- 혈전증이 의심되는 증상
- 하지의 통증 · 부종 · 마비 · 발적 · 열감, 두통, 구기 · 구토 등
- 혈전증이 의심되는 증상
- 혈전증의 위험이 높아지는 상태(몸을 움직일 수 없는 상태, 현저한 혈압 상승, 탈수 등)이 인정되는 경우는, 투여를 중지하는 등 적절한 처치를 실시하는 것.
- 본제 복용자에게는, 투여 개시시 및 계속시에 이하에 대해 설명할 것.
- 혈전증은 생명에 관련된 경과를 따르는 일이 있다.
- 혈전증이 의심되는 증상이 나타난 경우나, 혈전증의 리스크가 높아지는 상태가 된 경우는, 증상·상태가 경도라도 즉시 복용을 중지해 의사등에 상담하는 것.
- 혈전증을 의심하고 다른 의료기관을 진찰할 때는, 본제의 사용을 의사에게 고지해, 본제에 의한 혈전증을 염두에 둔 진찰을 받을 수 있도록 하는 것.
- 본제 복용 중에 부득이하게 수술이 필요하다고 판단되는 경우에는 혈전증의 예방에 충분히 배려할 것.
- 연령 및 흡연량에 의해 심혈관계의 심각한 부작용의 위험성이 증대한다는 보고가 있다. 따라서 본제 복용자에게는 금연하도록 지도할 것.
- 이 약의 투여에는 복용자의 병력 조사 및 검진이 필요하다. 이 검사에는 혈압 측정, 유방 및 복부 검사 및 임상 검사가 포함됩니다. 또, 투여중은 6개월마다의 검진을 실시하는 것.
- 본제 투여 개시 전 및 투여중은, 1년에 1회 이상, 자궁·난소를 중심으로 한 골반 내장기의 검사를 실시할 것. 1년에 1회, 자궁경부의 세포진의 실시를 고려하는 것.
- 유방암의 검사는, 복용자에게 자기 검진을 실시하도록 지도하는 것.
- 복용중에 부정성기 출혈이 발현된 경우, 통상은 투여 계속 중에 소실되지만, 장기간 지속하는 경우는, 질 세포 진단 등의 검사로 악성 질환에 의한 것이 아닌 것을 확인 후, 투여하는 것 .
조성·성상
조성
마블론 21
| 마블론 21/28 공통 | ||
| 유효성분 | 1 정중 데소게스트렐 0.15 mg |
|
| 1 정중 일국 에티닐에스트라디올 0.03 mg |
||
| 첨가제 | 발레이쇼 전분, 포비돈, 스테아르산, 경질 무수 규산, 토코페롤, 유당 수화물, 히프로멜로스, 마크로골 400, 산화티탄, 탈크 | |
마블론 28
| 마블론 21/28 공통 | ||
| 유효성분 | 1 정중 데소게스트렐 0.15 mg |
|
| 1 정중 일국 에티닐에스트라디올 0.03 mg |
||
| 첨가제 | 발레이쇼 전분, 포비돈, 스테아르산, 경질 무수 규산, 토코페롤, 유당 수화물, 히프로멜로스, 마크로골 400, 산화티탄, 탈크 | |
| 마블론 28만 | ||
| 유효성분 | 1 정중 데소게스트렐 함유하지 않고 |
|
| 1 정중 일국 에티닐에스트라디올 함유하지 않고 |
||
| 첨가제 | 옥수수 전분, 스테아르산마그네슘, 유당 수화물, 히프로멜로스, 마크로골 400, 산화티탄, 활석, 황색 삼이산화철, 식용 청색 2호 알루미늄 레이크 | |
제형의 특성
마블론 21
| 마블론 21/28 공통 | ||
| 투약 형태 | 필름 코팅 정제 | |
| 색조 | 백색 | |
| 외형 | 표면 |  |
| 뒷면 |  |
|
| 측면 | ||
| 크기 | 지름 | 5.0mm |
| 두께 | 2.9mm | |
| 질량 | 66mg | |
| 식별 코드 | TR5 ☆ORGANON |
|
| 정제 수 | 21정 | |
마블론 28
| 마블론 21/28 공통 | ||
| 투약 형태 | 필름 코팅 정제 | |
| 색조 | 백색 | |
| 외형 | 표면 |  |
| 뒷면 |  |
|
| 측면 | ||
| 크기 | 지름 | 5.0mm |
| 두께 | 2.9mm | |
| 질량 | 66mg | |
| 식별 코드 | TR5 ☆ORGANON |
|
| 정제 수 | 21정 | |
| 마블론 28만 | ||
| 투약 형태 | 필름 코팅정[플라시보정] | |
| 색조 | 녹색 | |
| 외형 | 표면 |  |
| 뒷면 |  |
|
| 측면 | ||
| 크기 | 지름 | 5.0mm |
| 두께 | 2.8mm | |
| 질량 | 65mg | |
| 식별 코드 | KH2 ☆ORGANON |
|
| 정제 수 | 7정 | |
병용 금기(병용하지 않는 것)
| 약제명 등 | 임상 증상 · 조치 방법 | 기전·위험 인자 |
옴비타스빌 수화물, 파리타 프리빌 수화물, 리토나비르 제제
|
에티닐에스트라디올 함유 경구 피임제를 병용한 환자에서 ALT 상승이 고주파로 관찰되었다. 또한, 옴비타스빌 수화물·파리타프레비르 수화물·리토나비르 배합제 치료 종료의 약 2주일 후부터 본제의 투여를 재개할 수 있다. |
기전 불명 |
병용주의(병용에 주의할 것)
| 약제명 등 | 임상 증상 · 조치 방법 | 기전·위험 인자 |
부신피질호르몬
삼환계 항우울제
셀레기린 하이드로클로라이드 |
이들 약제의 작용이 향상될 우려가 있다. | 이 약은 이들 약제의 대사를 억제하는 것으로 생각된다. |
| 리팜피신 바르비툴산계 제제
히단토인계 제제
카르바 마제핀 |
이 약의 효과 감소 및 부정성 기 출혈의 발현률이 증가 할 수 있습니다. | 이들 약제는 약물 대사 효소를 유도하여 본제의 대사를 촉진시키는 것으로 생각된다. |
테트라사이클린계 항생제
페니실린계 항생제
|
이 약의 효과 감소 및 부정성 기 출혈의 발현률이 증가 할 수 있습니다. | 이들 약제는 장내 세균총을 변화시켜 본제의 장간 순환에 의한 재흡수를 억제하는 것으로 생각된다. |
| 테르비나핀 염산염 | 황체 호르몬·난포 호르몬 배합제와의 병용으로 월경 이상이 나타났다는 보고가 있다. | 기전 불명 |
Gn-RH 유도체
|
이들 약제의 작용을 감약할 우려가 있다. | 이들 약제는 성 호르몬의 분비를 저하시킴으로써 약효를 나타내기 때문에, 성 호르몬인 본제의 투여에 의해 이들 약제의 효과를 감약할 가능성이 생각된다. |
혈당 강하제
|
혈당 강하제의 작용이 약화될 수 있다. 혈당치 기타 환자의 상태를 충분히 관찰하고, 혈당강하제의 용량을 조절하는 등 주의한다. | 본 제제는 내당능을 저하시켜, 혈당 강하제의 작용을 감약시키는 것으로 생각된다. |
| 라모트리긴 | 경구 피임제와의 병용으로 라모트리긴의 혈중 농도가 감소했다는 보고가 있으므로, 라모트리긴 유지 용량 투여 중에 본제를 투여 개시 또는 중지하는 경우는 라모트리긴의 용량 조절을 고려할 것. | 간에서 라모트리긴의 글루쿠론산 접합이 촉진된다. |
| 모르핀 살리실산 |
이들 약제의 혈중 농도가 저하될 우려가 있다. | 본 약제는 이들 약제의 글루쿠론산 접합을 촉진시키는 것으로 생각된다. |
| HIV 감염 치료제 HIV 프로테아제 억제제
비뉴클레오시드계 역전사효소 억제제
|
본제의 작용이 감약할 우려가 있다. | 에티닐에스트라디올의 AUC가 감소한다. |
|
본제의 작용이 감약할 우려가 있다. | 데소게스트렐의 활성 대사산물인 에토노게스트렐의 혈중 농도가 감소한다. |
|
본제의 혈중 농도가 상승할 우려가 있다. | 에트라비린은 본제의 대사효소(CYP2C9)를 억제하는 것으로 생각된다. |
HCV 감염증 치료제
|
본제의 작용이 감약할 우려가 있다. | 에티닐에스트라디올의 AUC가 감소한다. |
| 플루코나졸 이트라코나졸 |
본제의 혈중 농도가 상승할 우려가 있다. | 이 약의 대사 효소 (CYP3A4)를 억제하는 것으로 생각된다. |
| 볼리코나졸 | 본제의 혈중 농도가 상승할 우려가 있다. 볼리코나졸의 혈중 농도가 상승할 우려가 있다. | 보리코나졸은 본제의 대사효소(CYP3A4)를 억제하는 것으로 생각된다. 이 약은 볼리코나졸의 대사 효소 (CYP2C19)를 억제하는 것으로 생각된다. |
| 아세트아미노펜 | 본제의 혈중 농도가 상승할 우려가 있다. 아세트아미노펜의 혈중 농도가 저하될 우려가 있다. | 아세트아미노펜은 에티닐에스트라디올의 황산 접합을 억제하는 것으로 생각된다. 이 약은 간에서 아세트 아미노펜의 글루 쿠로 네이트 접합을 촉진하는 것으로 생각된다. |
| 세이요우오토 그리스 우(St. John’s Wort, 세인트 존스 워트) 함유 식품 |
본제의 효과의 감약화 및 부정성기 출혈의 발현률이 증대할 우려가 있기 때문에, 본제 투여시에는 볶음밥 그리스 함유 식품을 섭취하지 않도록 주의할 것. | 이 식품은 약물 대사 효소를 유도하여 본제의 대사를 촉진하는 것으로 생각된다. |
부작용
다음의 부작용이 나타날 수 있으므로, 관찰을 충분히 실시해, 이상이 인정되었을 경우에는 투여를 중지하는 등 적절한 처치를 실시하는 것.
심각한 부작용
혈전증(사지, 폐, 심장, 뇌, 망막 등)(빈도 불명)
하지의 급격한 통증 · 부종, 갑작스런 호흡 곤란, 흉통, 심한 두통, 사지의 탈력 · 마비, 구문 장애, 급성 시력 장애 등의 증상이 나타난 경우에는 즉시 투여를 중지하고 적절한 조치를 취할 것 .
기타 부작용
| 5% 이상 | 0.1 ~ 5% 미만 | 빈도 불명 | |
| 과민증 | 발진 | ||
| 눈 | 시력 장애 | 망막 혈류 장애로 인한 시력 장애 | |
| 간 | 간기능 이상, AST 상승, ALT 상승 | 황달 | |
| 신진 대사 | 나트륨이나 체액의 저류에 의한 부종, 체중 증가 | ||
| 생식계 | 부정성기 출혈 (파탄 출혈, 점상 출혈), 하역, 월경 과다, 월경통, 성교통, 리비도 감소 | ||
| 유방 | 유방통 | 유방 긴만(감) | 우유 누출 |
| 순환기 | 기외 수축, 혈압 상승, 동계 | ||
| 소화기 | 오심 | 구토, 설사, 복통, 변비, 식욕 감퇴, 가슴앓이, 복부 팽만감 | |
| 호흡기 | 인두통, 기침 | ||
| 정신 신경계 | 두통 | 현기증, 졸음 | 우울증, 짜증, 편두통 |
| 피부 | 여드름, 습진, 가려움, 색소 침착, 홍반 | 탈모 | |
| 근골격 | 허리 통증, 다리 통증, 어깨 결림, 손가락의 경직 | ||
| 기타 | 권태감, 구강, 안면 부종, 흉통, 백혈구 감소, 알도스테론 상승 |
주) 장시간 태양광을 받지 않도록 주의할 것.
임상 검사 결과에 미치는 영향
함유 된 에티닐 에스트라 디올의 작용에 의한 혈청 단백질 (코르티코이드 결합 글로불린, 사이 록신 결합 글로불린 등)의 증가에 의해 총 코르티솔, 총 T3 , 총 T4 의 상승이 보일 수있다. 또한, 이러한 자유형은 변화하지 않는다고 여겨진다. 이들 검사치의 판정에 있어서는 주의할 것.
적용상의 주의
약제 교부시의 주의
PTP 포장의 약제는 PTP 시트에서 꺼내 복용하도록 지도하는 것. PTP 시트의 오음에 의해, 딱딱한 예각부가 식도 점막에 자입하고, 또한 천공을 일으켜 종격동염 등의 심각한 합병증이 병발하는 경우가 있다.
기타 주의
임상 사용에 기초한 정보
- 외국에서의 역학조사 결과 정맥혈전증의 위험은 경구피임제를 복용하는 여성은 복용하지 않은 여성에 비해 3.25~4.0배 높아진다는 보고가 있다. 또한 정맥 혈전증의 위험은 경구 피임제 복용 개시 첫 1 년 동안 가장 높다는보고가 있습니다. 게다가 외국에서의 대규모 시판 후 조사의 결과, 처음으로 경구 피임제의 복용을 개시했을 때뿐만 아니라, 4주간 이상의 중단 후에 복용을 재개했을 때 또는 4주간 이상의 중단 후에 다른 경구 피임제 로 전환했을 때에도 정맥 혈전증의 리스크가 상승하고, 그 리스크는 복용 개시 후 3개월간이 특히 높다는 보고가 있다.
또한, 1995년~1996년에 데소게스트렐을 포함한 경구 피임제는 레보놀게스트렐 등의 경구 피임제에 비해 정맥 혈전증의 상대 위험률을 증가시키는 것을 시사하는 보고(레보놀게스트렐 등의 경구 피임제 에 의한 정맥 혈전증의 환자가 1년간에 1만명당 1명인데 대해 데소게스트렐을 포함한 경구 피임제에서는 2명이 된다)가 있다. 덧붙여서, 임신에 의한 정맥 혈전의 발병은 1년간에 1만명당 6명으로 알려져 있다. - 외국에서의 역학조사의 결과, 경구피임제의 복용에 의해 유방암 및 자궁경부암이 될 가능성이 높아진다는 보고가 있다.
- 외국에서 경구피임제를 2년 이상 복용한 경우 양성 간종양이 10만명당 3.4명 발생한다는 보고가 있다. 또한 종양 파열로 복강 내 출혈을 일으킬 수 있습니다. 한편, 악성 간종양(간암)의 발생률은 매우 낮아 100만명당 1명에 못 미친다.
- 외국에서 경구피임제 복용으로 전신성 홍 반성 루푸스(SLE)의 악화, 아나필락시스 유사 증상, 용혈성 요독증후군(HUS), 혈관부종이 나타났다는 보고가 있다.
- 외국에서 경구 피임제 복용에 의한 각막 두께의 변화 등에 의해 콘택트 렌즈가 잘 조정되지 않기 때문에, 시력·시야의 변화, 착용시의 불쾌감 등이 보였다는 보고가 있다.
약동학
혈중 농도
건강한 성인 여성에게 경구 투여하면 소화관으로부터의 흡수가 신속하고 활성 대사 산물인 3-케토-데소게스트렐 및 에티닐에스트라디올의 혈청 농도는 투여 후 약 2시간 내에 최고치에 도달한다. 또한, 반복 투여한 경우, 3-케토-데소게스트렐 및 에티닐에스트라디올의 혈청중 농도는 거의 15일째에 정상상태에 이르고, 21일 투여 후의 소실상반감기는 각각 22.0, 23.7시간이었다.
| 표 21 일 연속 경구 투여 후 약동학 파라미터 | ||||
| AUC (pmol·hr/mL) |
t 1/2 (hr) |
C max (pmol/mL) |
T max (hr) |
|
| 3-케토-데소게스트렐 | 97.2±36.8 | 22.0±9.6 | 12.12±5.49 | 1.2±0.6 |
| 에티닐에스트라디올 | 11.7±3.3 | 23.7±8.8 | 1.18±0.32 | 1.1±0.6 |
배설
건강 성인 여성에게 3 H-표지된 데소게스트렐과 에티닐에스트라디올을 경구 투여한 경우, 투여 후 8일째까지 소변 중에는 약 48%, 배설물 중에는 약 35%가 배설되었다(외국인 데이터).
임상 성적
효능 및 안전성에 관한 시험
국내 임상시험
피임을 희망하는 여성 992례에 대해 실시된 임상시험에 있어서, 약제에 기인하는 것으로 판정된 임신이 1예로 보였고, 피임효과는 99.9%, 연복용주기(14,088주기)에서의 Pearl index는 0.085였다 .
피임을 희망하는 여성 1,011례(14,378주기) 중, 부작용이 보고된 것은, 258례(25.5%)로, 주된 것은, 구역 119례(11.8%), 유방통 85례(8.4%) , 두통 59례(5.8%), 부정성기 출혈 24례(2.4%), 구토 23례(2.3%), 권태감 12례(1.2%), 설사 11례(1.1%), 복통 10례(1.0%) )이었다. 또한, 임상 검사치의 이상이 보고된 것은 AST 상승 및 ALT 상승 2례, 백혈구 수 감소 1례, 알도스테론 상승 1례의 총 4례였다.
기타
각종 피임법 사용 개시 1년간의 실패율(임신률)은 이하와 같다 .
| 방법 | 이상적인 사용 (%) |
일반 사용 ) (%) |
| 경구 피임제 | 0.3 | 9 |
| 레보놀 게스트렐 방출 IUS | 0.2 | 0.2 |
| 구리 부가 IUD | 0.6 | 0.8 |
| 콘돔 | 2 | 18 |
| 리듬법 | 0.4~5 | 24 |
| 여성 피임 수술 | 0.5 | 0.5 |
| 남성 피임 수술 | 0.10 | 0.15 |
| 피임하지 않고 | 85 | 85 |
| IUS : 자궁내 시스템 IUD : 자궁내 피임 도구
주1) 선택한 피임법을 올바르게 계속해서 사용하고 있음에도 불구하고 임신해 버린 경우 주2) 선택한 피임법을 사용하고 있음에도 불구하고 임신해 버린 경우 |
||
약효 약리
작용 메커니즘
본제는 배란 억제 작용을 주작용으로 하고, 자궁내막 변화에 의한 착상 억제 작용 및 경관 점액 변화에 의한 정자 통과성 억제 등에 의해 피임 효과를 발휘한다.
배란 억제 작용
본제의 연속 복용에 의해, 혈중의 황체·난포 호르몬치는 일정하게 유지된다. 그 결과, 뇌하수체 전엽 gonadotropin 분비의 생리적 패턴이 억제되고, gonadotropin 분비의 감소에 의해 배란이 억제된다.
자궁 내막의 성상 변화에 의한 착상 억제 작용
이 약의 연속 복용은 자궁 내막의 성상을 변화시켜 수정란의 착상을 억제합니다.
자궁 경관 점액의 변화에 의한 정자 통과성 억제 작용
본제의 연속 복용에 의해, 자궁 경관 점액의 성상이나 조성의 변화가 일어나, 자궁강 내로의 정자의 통과성이 저해된다.
활성 성분에 관한 물리 화학적 발견
데소게스트렐
일반 이름
데소게스트렐(Desogestrel)
화학명
(+)-17α-Ethynyl-18-methyl-11-methylene-4-estren-17-ol
분자식
C 22 H 30 O
분자량
310.47
성상
백색 결정 성 분말로 냄새가 없습니다.
아세톤, 디클로로 메탄 또는 테트라 히드로 푸란에 매우 녹기 쉽고, 에탄올 (99.5) 또는 디 에틸 에테르에 녹기 쉽고 헥산에 약간 녹기 쉽고 물에 거의 녹지 않습니다.
화학 구조식
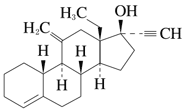
융점
110~112℃
에티닐에스트라디올
일반 이름
에티닐에스트라디올(Ethinylestradiol)
화학명
19-Nor-17α-pregna-1,3,5(10)-triene-20-yne-3,17-diol
분자식
C 20 H 24 O 2
분자량
296.40
성상
백색 내지 미황색의 결정 또는 결정성의 분말로, 냄새는 없다.
피리딘 또는 테트라 히드로 푸란에 녹기 쉽고 에탄올 (95) 또는 디 에틸 에테르에 약간 녹기 쉽고 물에 거의 녹지 않습니다. 수산화나트륨 시액에 녹는다.
화학 구조식
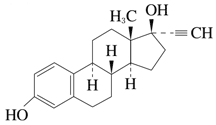
융점
180~186℃ 또는 142~146℃
취급상의 주의
본제는 소아의 손이 닿지 않는 장소에 보관할 것.
포장
- <마블론 21>
210정[21정(PTP)×10]
1,050정[21정(PTP)×50]
- <마블론 28>
280정[28정(PTP)×10]
1,400정[28정(PTP)×50]
마블론 21/마블론 28
작성 또는 개정 연월
| * | 2021년 9월 개정 (제2판) |
| 2019년 10월 개정 (제1판) |
일본 표준 상품 분류 번호
872549
약효 분류명
경구 피임제
승인 등
마블론 21
판매 이름 코드
YJ 코드
254910CF1025
판매명 영어 표기
MARVELON 21 Tablets
판매 이름 히라가나
마베론
승인 번호 등
승인 번호
21100AMY00154000
판매 개시 연월
2005년 4월
저법・유효기간
저법
실온 저장
유효기간
3년
규제 구분
처방전 의약품
주 1) 주의―의사의 처방에 의해 사용하는 것
마블론 28
판매 이름 코드
YJ 코드
254910CF2021
판매명 영어 표기
MARVELON 28 Tablets
판매 이름 히라가나
마베론
승인 번호 등
승인 번호
21100AMY00155000
판매 개시 연월
2006년 12월
저법・유효기간
저법
실온 저장
유효기간
3년
규제 구분
처방전 의약품
주 2) 주의―의사의 처방에 의해 사용하는 것
주요 문헌
1) 미즈노 마사히코 외 . 일본 불임 학회지 . 1991; 36 : 35-48.
2) Viinikka L, et al. Acta Endocrinol. 1980; 93: 375-9.
3) 미즈노 마사히코 외 . 산과 및 부인과 . 1990; 57 : 2507-32.
4) 타카기 번부 외 . 기초와 임상 . 1991; 25: 2807-16.
5) 미즈노 마사히코 외 . 산과 및 부인과 . 1992; 59 : 149-59.
6) Hatcher RA, et al. Contraceptive Technology. Twentieth Revised Edition. NewYork: Ardent Media; 2011
7) Cullberg G, et al. Acta Obst Gynecol Scand. 1982; Suppl. 111: 29-38.
8) Mall-Haefeli M, et al. Geburtshilfe Frauenheilkd. 1984; 44: 177-9.
9) Viinikka L, et al. Acta Endocrinol. 1976; 83: 429-38.
10) 안전성에 관한 참고 자료 종양에 관한 사항
• Collaborative Group on Hormonal Factors in Breast Cancer : Lancet, 347 : 1713-1727, 1996
• WHO : Int J. Cancer, 55 : 228-236, 1993
• Ursin, G. et al. : Lancet, 344 : 1390-1394, 1994
• Ye, Z. et al. : Int J. Epidemiol., 24 : 19-26, 1995
• Thomas, D. B. et al. : Am. J. Epidemiol., 14 : 281-289, 1996
• 오가와 시게오 등 : 필수산부인과학 개정 제 4 판 , p.390, p.395-396, 남강당 , 1996
• Edmondson, H. A. et al .N. Engl. J. Med., 294 : 470-472, 1976
• Neuberger, J. et al. : Br. Med. J., 292 : 1355-1357
, 1986 618-623, 메디컬뷰사 , 1987
• 유방암검진(일본대암협회편 , 사회 보험 출판사 , 1984 )
• 유방암집단검진 안내(유방암연구회편 , 시노하라 출판 , 1987 ) 저널 , 1995 ) • Becker, T. M. et al. : Int. J. Epidemiol., 23 : 913-922 , 1994 • Parazzini , F. et al .
• Zondervan ,
K. T. et al . _ _ _ _ _ , 77 : 219-223, 1998 • Rooks, J. B. et al. : JAMA , 242 : 644-648 , 1979 • Corfman, PA : Contraception, 37 : 433-455, 1988 • Dis., 4 : 147-157, 1984 • Forman, D. et al. : Br. Med. J., 292 : 1357-1361, 1986 • WHO :
Int. J. Cancer, 43 : 254-259, 1989
• The Collaborative MILTS ( Multi-centre International Liver Tumor Study ): Contraception, 56 : 275-284, 1997
11) 안전성에 관한 참고 자료 심혈관계에 관한 사항
• WHO : Lancet, 346 : 1575-1582, 1995
• Spitzer, W. O. et al. : Br. Med. J., 312 : 83-88, 1996
• WHO : Lancet , 348 : 498-505, 1996
• WHO : Lancet, 348 : 505-510 , 1996
• Petitti, D. B. et al. : N. Engl. J. Med., 335 : 8-15, 1996
• WHO : 1202-1209, 1997 • Lewis, M. A. et al. : Contraception, 56 : 129-140, 1997 • WHO Special Program of Research
: Br. J. Obstet. Gynaecol., 98 : 1117-1128, 1991
• Jespersen, J. et al. : Am. J. Obstet. Gynecol., 163 : 396-403, 1990
• Layde, P. M. et al . Lancet, I : 541-546, 1981
• Stadel, B. V. : N. Engl. J. Med., 305 : 672-677, 1981
• 카자마 아츠미 : Biomedical Perspectives, 6 : 85-89, 1997
• Bloemenka : Lancet, 346 : 1593-1596, 1995
• 마루야마 정로 : 혈전과 순환 , 4 : 21-23, 1996
• 노지마 순삼 등 : 임상 병리 , 46 :1181-1187, 1998
• Robinson, G. E. et al. : Br. Med . J., 302 : 269-271 , 1991
• Vessey , M. P. et al . 시노기 노부토시: medicina, 33 : 1308-1310, 1996 • Gibbs, N. M. : Br. J. Surg., 45 : 209-236, 1957 • Kawasaki, T. et al. : Thrombosis Res., 79 : 1 , 1995 • 타카기 번부 등 : 綜合臨床, 34 : 1115-1119, 1985 • Jain, A. K. et al. : Studies in Family Planning, 8 : 50-54, 1977 •
「데소게스트렐 또는 게스트덴 함유 경구피임약에 관한 유럽 의약품 위원회( CPMP ) 성명( Position Statement )」, CPMP /374/96, 1996 년 4 월 17 일 의치약 출판 , 1994 • 와키자카 유이치 : 병태 혈학, p.477 , 남강당 , 1978 • Farley, T. M. M. et al. : Contraception , 57 : 211-230 , 1998 Med. J., 315 : 1502-1504, 1997
12) 안전성에 관한 참고자료 차세대에의 영향에 관한 사항
• 야스다 요시코 등 : 의학의 아유미 , 98 : 537-538, 1976
• 야스다 요시코 등 : 의학의 아유미 et al . _ _ _ _ _ _ _ _ _ _ _ 559-573, 1990 • Corfman, P. A. : Contraception, 37 : 433-455, 1988 • Heinonen, O. P. et al. : N. Engl. J. Med., 296 : 67-70, 1977
• Harlap, S. et al. : Obstet. Gynecol., 55 : 447-452 , 1980
• Savolainen, E. et al. : Am. J. Obstet . et al. : Teratology , 21 : 225-239 , 1980 • Rothman, K. J. et al. : Am. J. Epidemiol., 109 : 433-439 , 1979 • 상견 4756, 1990 • 하라다 시오오 등 : 약리와 치료 , 19 : S965-S999, 1991 • Kwarta , Jr. R. F. et al. : 응용 약리 , 42 : 327-340, 1991
, 36 : 284-299, 1991
• 선천이상조사 20 년의 아유미 : 일본모성보호의협회 , 1993
• 도쿄도립병산원에서 선천이상 출산 모니터링 조사
• Li, D. K. et al. : Teratology, 51 : 30-36 , 1995
• Kim, M. R. et al. : Am . J. Obstet . Gynecol ., 172 : 1042-1043,
1995 Can. Med. Assoc. J., 103 : 343-348, 1970 • Lauritsen, J. G. : Acta Obstet. Gynecol. Scand., 54 : 261-264, 1975 • Dhadial, R. K. et al .
Lancet, Ⅱ : 20-21, 1970
• Boue , J. et al. : Teratology , 12 : 11-26 ,
1975 . : Teratology, 31 : 381-387, 1985 • Depue, R. H. et al. : J. Natl. Cancer Inst., 71 : 1151-1155, 1983 • Henderson, B. E. et al. : Int. J. Cancer 598-602, 1979 • Brown, L. M. et al. : Cancer Res., 46 : 4812-4816, 1986 • Moss, A. R. et al .: Am. J. Epidemiol., 124 :
39-52, 1986
13) 안전에 관한 참고 자료 임신 기능에 관한 사항
• Woutersz, T. B. : J. Reprod. Med., 26 : 615-620, 1981
• Royal College of General Practitioners Oral Contraceptives and Health, p.71-77, Pitman Medical, London, 1974
• Mosher, W. D. et al .: Fertil . Steril., 56 : 192-193 , 1991
• Chasan-Taber, L. et al.: Am . J. Epidemiol.
14) 안전성에 관한 참고 자료 기타
• 후생성 의약품 부작용 정보 , No.28 , 33-35, 1977
• Fisch , I. R. et al . Oto-Rino-Laringol., 41 : 46-50, 1975 • Drill, V. A. : Am. J. Obstet. Gynecol., 119 : 165-174, 1974 • Orellana-Alcalde, J. M. et al. : Lancet , Ⅱ 1278-1280, 1966 • Koide, S. S. et al .: J. Reprod. Med., 15 : 214-224, 1975 • Nilsson, S .: Contraception, 17 : 131-139, 1978
• 요시모토 마사아키: 호르몬과 임상 , 44 : 597-605, 1996
• Chasan-Taber, L. et al. : Circulation, 94 : 483-489, 1996
• Godsland, I. F. et al. : J. Clin. Endocrin. Metab., 74 : 64-70, 1992
• 니노미야 료코 등 : 임상 피부과 , 48 : 281-283 , 1994
• 강기 , p.176 , p.1450 , 1977 • 오카다 히로지 : 스테로이드 요법의 본문
853-861, 1986
• Burckhardt, P. : Hormone Res., 6 : 321-328, 1975
• Crook, D. et al. : Am. J. Obstet. Gynecol., 158 : 1612-1620, 1988
• Fre BM et al .: Eur. J. Clin. Pharmacol., 26 : 505-511, 1984
• Abernethy , D. R. et al .: Clin . Pharmacol . Ther . 시클로스포린 첨부 문서 • Reimers, D. et al. : Prax . Pneumol. , 25 : 255-262 , 1971 • Back, D. J. et al .
• Back, D. J. et al .: Br. J. Pharmacol. , 69 : 441-452, 1980
• Back, D. J. et al .: Br. J. Clin. Pharmacol . et al. : Br. J. Clin. Pharmacol., 30 : 892-896, 1990 • Back , D. J. et al. : J. Steroid . 부세렐린 아세테이트 첨부 문서 • Steel, J. M. : J. Fam. Plan. Doctors, 3 : 77-78, 1978 • 넬피나비르 메실레이트 첨부 문서 • Ouellet, D. et al. : Br. J. Clin. Pharmacol., 46:
111-116, 1998
• 네비라핀 첨부 문서
• 히가키 가키코 : 오늘의 치료 지침 , p713, 의학 서원 , 1999
• Van Vange, N. et al. : Contraception, 41 : 345-352, 1990
• 야구치 , 40 : 14-20, 1988
• Schatz , D. L. et al. : Can. Med. Assoc. J., 99 , 882-886,
1968 V. et al .: Br. Med. J., 318 : 96-100, 1999 • Mostad , S. B. et al .: Lancet, 350 : 922-927, 1997
: Oral Contraceptives and Health, p.31, Pitman Medical, London, 1974
• Bray, R. S. : Contraception, 13 : 417-425 , 1976
• Keller, A. J. et al. : Obstet . • Gerretsen, G. et al. : Contraception, 22 : 25-29, 1980 • Baker, D. A. et al . : Contraception , 32 : 377-382 , 1985 , 1988 • Baker, D. A. et al. : Contraception, 39 : 119-124, 1989 • Scanlan, J. M. et al .
Psychoneuroendocrinology, 20 : 281-287, 1995
15) 효능에 관한 참고 자료 피임 효과에 관한 사항
• Hatcher, R. A. et al. : Contraceptive Technology : Twentieth Revised Edition. New York : Ardent Media, : p . 779-861,
2011 20 : 61-69, 1979
• Chowdhury, V. 등 : Contraception, 22 : 241-247, 1980
• Sparrow, M. J. : N. Z. Med. J., 100 : 102-105, 1987
16) 유효성에 관한 참고 자료 인공 임신 낙태에 관한 자료
• 2005 년 모체 보호 통계 보고(후생성 장관 관방 통계 정보부 인구 동태 통계과) •
매일 신문 인구 문제 조사회(제 23 회 전국 가족 계획 여론 조사 보고서 더 개편)
• Determinants of contraceptive use
• United Nations : Demographic Yearbook 1996 판 . ©1998
17) 유효성에 관한 참고 자료 부효용에 관한 자료
• The Cancer and Steroid Hormone Study of the Centers for Disease Control and the National Institute of Child Health and Human Development : N. Engl. J. Med., 316 : 650-655, 1987
• Narod, S. A. et al.: N. Engl. J. Med., 339 : 424-428 , 1998
• The
Centers for Disease Control Cancer and Steroid Hormone Study Steroid Hormone Study of the Centers for Disease Control and the National Institute of Child Health and Human Development : JAMA, 257 : 796-800, 1987
• Schlesselman, J. J. :Hum. Reprod., 12 : 1851-1863, 1997
• Royal College of General Practitioners : Oral Contraceptives and Health, p.22, p.61, Pitman Medical, London, 1974
• Connel, E. B. et al. : J. Reprod. Med., 29 : 513-523, 1984
• Lanes, S. F. et al .: Am. J. Obstet. Gynecol., 166 : 956-961, 1992
• Vessey, M. et al .: J. Biosoc. Sci., 8 : 373-427, 1976
• Westrom, L. : Am. J. Obstet. Gynecol., 138 : 880-892, 1980
• Rubin, G. L. et al. : Am. J. Obstet. Gynecol., 144 : 63 635, 1982
• Brinton, L. A. et al. : Am. J. Epidemiol., 113 : 203-214, 1981
문헌 청구처 및 문의처
오가논 주식회사 고객 지원 센터
도쿄도 미나토구 미나미아오야마 1-24-3
무료 다이얼 0120-095-213
보험급여상의 주의
본제는 보험급여의 대상이 되지 않는다(약가 기준 미수재).
제조판매업자 등
제조 판매원
오가논 주식회사
도쿄도 미나토구 미나미아오야마 1-24-3


コメント